
УГЛЕРОД
УГЛЕРОД (С), хим. элемент IV группы периодической системы, атомный номер 6, атомный вес 12,010.
Известно пять изотопов У. с массовыми числами (атомными весами) 10, 11, 12, 13 и 14 (С10, С11, С12, С13 и С14). Обычный природный У. состоит из смеси стабильных (нерадиоактивных) изотопов С12 и С13, с примерным соотношением 99:1. Изотопы С10, С11 и С14 радиоактивны и получаются искусственно в результате ядерных реакций. Только изотоп С14 присутствует в природных соединениях У. в виде следов.
В свободном состоянии У. встречается в виде кристаллических веществ - алмаза и графита. При обугливании органических веществ образуется аморфный У. (кокс, древесный и животный уголь и сажа), в к-рый входят также зола и нек-рые неразложившиеся до У. органические вещества (гл. обр., смолы). В земной коре У. содержится 0,13%. В природе он находится, гл. обр., в виде разнообразных неорганических и органических соединений.
Больше всего У. содержится в карбонатах, т. е. в солях угольной ("карбоновой") кислоты. Сюда относятся, напр., известняки, известковые туфы и мрамор, состоящие в основном из углекислого кальция, а также магнезит, состоящий, гл. обр., из углекислого магния. Имеются смешанные породы, в состав к-рых входят карбонаты кальция и магния (напр., доломиты, доломитизированные известняки), или те же карбонаты, но с большей или меньшей примесью других минералов, напр. глин (лёссы, мергеля). В нейтральных и щелочных почвах также содержатся карбонаты, количество к-рых может достигать 1 - 10% и больше от веса почвы.
В глубоких слоях земли содержатся соединения У. - карбиды: железа, никеля, кремния, бора и др. Эти карбиды, а также карбид кальция получают искусственно: карбид кальция - для добывания ацетилена при сварке и для приготовления азотного удобрения цианамида кальция; карбиды бора и кремния - для резцов и сверл взамен алмаза.
Много У. рассеяно в воздухе в форме углекислого газа и в виде этого же газа и солей угольной кислоты растворено в воде рек, озёр, морей и океанов. Горючие ископаемые также являются углеродистыми. Содержание У. в сгорающей части составляет у антрацита до 96%, у каменного угля до 80 - 90%, у бурого угля до 70%, у торфа до 57%. В нефти содержится ок. 80 - 87% У. Природные горючие газы также состоят из газообразных углеродистых соединений; В почвенном перегное (гумусе) содержится в ср. 58%, в древесине ок. 50%, а в растительных веществах ок. 45% углерода.
Атомы У. вступают в соединения не только с другими элементами, но и друг с другом, образуя многочисленные устойчивые цепные, разветвлённые и кольчатые структуры. Эта и другие особенности У. сделали его "главным носителем органической жизни" (Ф. Энгельс, Диалектика природы, 1952, стр. 201). Химических безуглеродных соединений известно всего несколько десятков тысяч, в то время как соединений У. насчитывается много сотен тысяч, причём с каждым годом число углеродистых соединений возрастает за счёт синтеза новых. Изучение углеродистых соединений выделилось в самостоятельный раздел химии, получивший название органической химии. Вначале химики могли выделять углеродистые соединения лишь из растительных и животных организмов или из их остатков. В 60-х годах прошлого века великий русский химик А. М. Бутлеров создал теорию строения углеродистых соединений. Трудами Н. Н. Зинина, А. М. Бутлерова и других русских химиков были заложены основы синтетической органической химии. Начав с синтеза мочевины, жиров и Сахаров, химики вскоре стали получать синтетические аминокислоты - составные части белковой молекулы и даже отдельные части белков, т. н. полипептиды, затем овладели синтезом многих витаминов, гормонов, активных групп ферментов и др. сложных и тонких органических образований.
Каждый атом У. способен присоединить 4 атома водорода или другого одновалентного элемента или 2 атома кислорода или другого двухвалентного элемента. При соединении с кислородом, т. е. при горении, образуется углекислый газ (двуокись углерода) СО2 со строением О=С=О. При недостатке кислорода образуется ядовитый угарный газ (окись углерода) СО. Окись углерода горюча и входит в состав генераторного газа (до 25%), водяного (до 40%) и смешанного (до 30%). При соединении с серой У. образует сероуглерод CS2, т. е. S=C=S.
Соединения У. с водородом называется углеводородами. Простейшим из них является метан (болотный газ) СН4, а за ним идёт этан СН3-СН3. Далее следуют пропан СН3·СН2·СН3, бутан СН3·СН2·СН2·СН3, пентан СН3·СН2·СН2·СН2·СН3, гексан СН3·СН2·СН2·СН2·СН2·СН3 и т. д. Кроме углеводородов цепного (линейного) строения, называемых жирными, с общей формулой СnH2n+2 существуют углеводороды кольчатого (циклического) строения с формулой СnН2n. Напр., наряду с нормальным гексаном известен циклогексан со след. строением молекул:
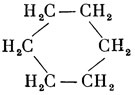
В указанных углеводородах все четыре связи (валентности) каждого атома углерода насыщены, поэтому такие углеводороды называются насыщенными, или предельными. Но имеются также и ненасыщенные, или непредельные, углеводороды, как жирные, напр. этилен СН2:СН2 и ацетилен СН⋮СН, так и циклические, напр. бензол.
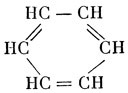
Все углеродистые соединения с двойными и тройными, т. е. ненасыщенными, связями обладают способностью присоединять к себе атомы хлора и других элементов. Напр., к молекуле бензола может присоединиться 6 атомов хлора, причём образуется гексахлорциклогексан С6Н6Сl6, соединение с инсектисидными свойствами, известное в практике под названием гексахлорана.
Атомы водорода в насыщенных углеродистых соединениях могут замещаться атомами других элементов. Напр., из соединений метана получают фумигант хлористый метил (метилхлорид) СН3Сl, хлороформ СHСl3, хлорпикрин CCl3NO2, четырёх-хлористый углерод ССl4, фосген СОСl2 и др., а из соединений этана - дихлорэтан С2Н4Сl2. Замещая три валентности У. одним атомом трёхвалентного азота, а четвёртую атомом водорода, получают чрезвычайно ядовитую синильную кислоту HCN или Н-C≡N, соли которой (цианиды, напр., цианистый натрий) употребляют для борьбы с вредителями р-ний. В соединениях с водородом и кислородом У. образует спирты (напр., метиловый, или древесный, СН3ОН, этиловый, или винный, С2Н5ОН), фенолы (напр., обыкновенный фенол, или карболовую кислоту, С6Н5ОН); углеводы [глюкозу C6H12O6, крахмал и клетчатки (С6Н10O5)n, сахарозу С12Н22О11 и др.]; органические кислоты (напр., уксусную СН3СООН, стеариновую СН3(СН2)16СООН и др.); эфиры (простые, напр. этиловый, или "серный", С2Н5ОС2Н5) и сложные (напр., уксусно-этиловый СН3СООС2Н5 и др.); к эфирам относятся также жиры, масла и воски; альдегиды (напр., формальдегид, или альдегид муравьиной кислоты, 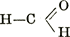 и др.). В соединениях с водородом, кислородом и азотом У. образует аминокислоты (напр., аминоуксусную, или гликокол CH2NH2-COOH, и др.), из к-рых построены белки; с азотом У. образует алкалоиды и др. азотистые органические соединения. Источником для пром. синтезов органических соединений служат уголь, нефть, древесина, хлопок.
и др.). В соединениях с водородом, кислородом и азотом У. образует аминокислоты (напр., аминоуксусную, или гликокол CH2NH2-COOH, и др.), из к-рых построены белки; с азотом У. образует алкалоиды и др. азотистые органические соединения. Источником для пром. синтезов органических соединений служат уголь, нефть, древесина, хлопок.
Большой научный и производственный интерес представляет круговорот У. в природе и хозяйстве. Зелёные р-ния земного шара усваивают в процессе фотосинтеза миллиарды тонн углерода в год. Углекислота, кроме того, связывается ежегодно в больлих количествах при образовании карбонатов. Но количество углекислого газа в атмосфере не уменьшается. Углекислый газ в огромных количествах выделяется р-ниями и ж-ными в процессе дыхания, микроорганизмами при брожениях, при других процессах разложения органических веществ, а также при вулканических извержениях, при выходе на поверхность углекислых источников. Много углекислого газа выделяется в результате хоз. деятельности человека - от сжигания топлива, обжига известняков и, наконец, в результате усиления процессов разложения органических веществ почвы при её обработке.
Литература - см. Углекислота.
Источники:
- Сельскохозяйственная энциклопедия. Т. 5 (Т - Я)/ Ред. коллегия: П. П. Лобанов (глав ред) [и др.]. Издание третье, переработанное - М., Государственное издательство сельскохозяйственной литературы, М. 1956, с. 663
|
ПОИСК:
|
© AGROLIB.RU, 2010-2022
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://agrolib.ru/ 'Библиотека по агрономии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://agrolib.ru/ 'Библиотека по агрономии'