
КРЕМНИЙ
КРЕМНИЙ (Si), хим. элемент IV группы периодической системы Менделеева, атомный номер 14, ат. вес 28,06. К. имеет 3 стабильных изотопа с массовыми числами 28, 29 и 30, на к-рые в природных соединениях кремния приходится соответственно 92,28, 4,67 и 3,05% общего количества К. Известны также 2 радиоактивных изотопа кремния с массовыми числами 27 и 31 (получаются искусственным путём с помощью ядерных реакций). К. весьма распространённый элемент; в составе земной коры ок. 26% К. В природе К. встречается, гл. обр., в виде соединений с кислородом, среди к-рых наиболее распространены двуокись кремния (SiО2) и соединения кремнекислоты с основаниями - силикаты, являющиеся главной составной частью горных пород и минеральной части почв. Кварцевый песок состоит из SiО2, а в состав глин входят минералы, содержащие соединения кремнекислоты с полуторными окислами (Al203,Fe203) и др. основаниями. Природная SiО2 - исходный продукт для получения др. соединений К. Металлический К. выделяется из SiО2 восстановлением при высокой темп-ре - магнием или алюминием. При накаливании смеси SiО2 с углем образуется соединение К. с углеродом - карбид К., или карборунд (SiC). Так же как и углерод, К. даёт соединения с галоидами (напр., газообразный SiF4) и с водородом. Кремневодороды, или силаны (SiH4, Si2H6, Si3H8 и т. д.), имеют нек-рое сходство по строению и физ. свойствам с углеводородами (первые члены ряда газообразны, более высоко молекулярные - жидкости). В отличие от углерода, образующего прочные связи в цепочках С - С, связь Si - Si (так же как и связь Si - Н) непрочна. Наоборот, связь К. с кислородом Si - О очень прочная, чем и объясняется устойчивость распространённых в природе кремнекислородных соединений.
В кислородных соединениях К. находится в виде групп SiО4, в к-рых один атом кремния окружён в тетраэдрической координации четырьмя атомами кислорода. Строение и свойства силикатов в значительной степени обусловлены характером сочетания этих групп между собой и ионами др. элементов. В наиболее основных силикатах изолированные группы SiО4 занимают определённые места в кристаллической решётке в сочетании с положительными ионами (Са, Mg и др.), к-рые нейтрализуют отрицательный заряд SiО4. У волокнистых силикатов (типа асбеста) группы SiО4 образуют пояса и цепочки, в к-рых связь осуществляется через общий кислород по типу
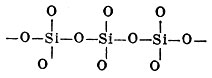
и т. д., чем объясняется характерная структура соответствующих минералов. У минералов типа слюд, а также каолина и др. минералов, входящих в состав глин, кремнекислородные группы образуют плоскостные сетки, в к-рых каждый тетраэдр SiО4 связан с тремя другими через общий кислород. Наконец, у минералов типа кварца происходит наиболее полная полимеризация путём образования объёмных ("вязаных") структур, в к-рых каждый кислород связан с двумя ионами кремния (состав кварца отвечает общей формуле SiО2). Аналогичного рода связи имеются в стекле, с тем отличием, что связанные между собой группы SiО4 располагаются здесь не в таком строгом порядке, как в кварце и др. кристаллах. Для кремнекислородных соединений характерна возможность частичного замещения в их структуре кремния на алюминий. При таком частичном замещении, вследствие меньшего положительного заряда иона алюминия по сравнению с кремнием, возникает отрицательный заряд, к-рый удерживает соответствующее количество др. ионов (Na, К, Са и др.). Такими замещениями обусловлено, в частности, наличие у нек-рых алюмосиликатов способности к обмену катионов.
К. входит в состав золы всех р-ний, иногда накапливаясь в очень больших количествах в клеточных оболочках нек-рых р-ний. Так, напр., зола соломы злаков содержит до 40%, а зола стеблей хвоща до 70% SiО2. Однако К. не является элементом, необходимым для питания р-ний в значительных количествах; в искусственных культурах удаётся выращивать р-ния без введения в питательную смесь К. Лишь в спец. условиях, при проведении опытов в металлических сосудах (а не стеклянных, из стенок к-рых К. частично переходит в раствор), удаётся наблюдать положительное действие малых доз К. на растения.
Большое количество кремнекислоты в виде кремнекислых солей кальция и магния содержится в нек-рых отходах металлургии (доменные шлаки). Основные доменные шлаки при внесении на кислых почвах действуют, гл. обр., как известковое удобрение. В некоторых опытах наблюдалось лучшее действие доменных шлаков, вносимых в качестве известкового удобрения на дерново-подзолистых почвах и краснозёмах по сравнению с действием углекислой извести.
Литература: Августиник А., Физическая химия силикатов. Л.-М., 1947; Белов Н., Структура ионных кристаллов и металлических фаз, [М.], 1947; Лашев Е., Слюда, ч. 1, М., 1948; Основные идеи геохимии, вып. 3. Под ред. А. Е. Ферсмана. Л., 1937.
Источники:
- Сельскохозяйственная энциклопедия. Т. 2 (Ж - К)/ Ред. коллегия: П. П. Лобанов (глав ред) [и др.]. Издание третье, переработанное - М., Государственное издательство сельскохозяйственной литературы, 1951, с. 624
|
ПОИСК:
|
© AGROLIB.RU, 2010-2022
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://agrolib.ru/ 'Библиотека по агрономии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://agrolib.ru/ 'Библиотека по агрономии'