
КОЛЛОИДЫ
КОЛЛОИДЫ, системы, состоящие из двух фаз (частей), разграниченных поверхностью раздела, в к-рых одна часть в мелкораздробленном (диспергированном) состоянии, более или менее равномерно распределена в другой. Первая называется дисперсной фазой, вторая дисперсионной средой. Размер частиц дисперсной фазы К. (коллоидных частиц) от 0,1 до 0,001 (л. Иногда в качестве верхнего предела размеров коллоидов принимают 0,2 и даже 0,5 ц. К. являются одним из видов дисперсных систем. Их внешние отличия от др. систем этого типа показаны в след. таблице.
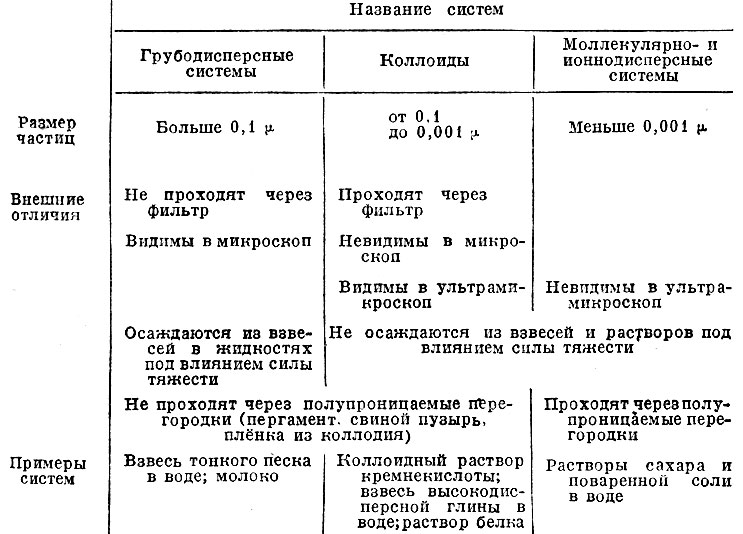
Дисперсные системы
К. классифицируют по агрегатному состоянию дисперсной фазы и дисперсионной среды на след. 8 типов: 1) твёрдое распределено в жидкости (напр., коллоидный раствор гидрата окиси железа); 2) жидкость - в жидкости (эмульсии); 3) газ в жидкости (высокодисперсные пены); 4) твёрдое - в твёрдом; 5) жидкость - в твёрдом и 6) газ - в твёрдом (4, 5 и 6 представлены нек-рыми минералами и сплавами); 7) твёрдое в газе и 8) жидкость в газе (7 и 8 - дым, туман, аэрозоль).
Типичным и наиболее изученным К. является коллоидный раствор, т. е. взвесь частиц указанных размеров в жидкости. Жидкие коллоидные растворы называются золи, студнеобразные - гели. В зависимости от дисперсионной среды различают гидрозоли (взвеси в воде), этерозоли (в эфире) и т. д. Коллоидные растворы обладают различной силой связи между дисперсной фазой и дисперсионной средой. По этому свойству их делят на лиофобные (для взвесей в воде - гидрофобные), у к-рых сродство фаз мало, и лиофильные (у водных взвесей - гидрофильные), у к-рых дисперсная фаза с трудом отделяется от дисперсионной среды. Первые часто называют суспензоиды, вторые - эмульсоиды. Многие К. занимают промежуточное положение. Частицы дисперсной фазы могут содержать различное количество молекул - от многих тысяч до одной. В последнем случае исчезает грань между коллоидными и истинными растворами и отсутствует поверхность раздела фаз. Однако растворы таких крупных молекул (макромолекулы, высокомолекулярные соединения) обладают многими свойствами коллоидных растворов.
Коллоидные частицы получают двумя путями: 1) диспергированием грубодисперсных частиц (напр., получение К. механическим дроблением, растворением высокомолекулярных соединений и пр.); 2) конденсацией молекул или ионов (напр. образование нерастворимых соединений в коллоидном состоянии из растворимых при различных хим. реакциях и др., а также конденсация водяного пара в туман). В природе коллоиды также образуются одним из этих путей, но чаще их комбинацией (напр., возникновение коллоидов при выветривании горных пород). От грубодисперсных частиц коллоиды очищают фильтрацией, отстаиванием и центрифугированием. От молекулярно- и ионорастворимых примесей - диализом, основанным на способности истинно растворённых веществ диффундировать через нек-рые перегородки, непроницаемые для коллоидных частиц. Ультрафильтрацией через такие перегородки дисперсионную среду очищают от высокодисперсных частиц.
Коллоидные частицы имеют сложное строение. В жидкости на их поверхности адсорбируются (см. Адсорбция) молекулы дисперсионной среды и растворённые" электролиты. Вместе с ними коллоидная частица образует мицеллу. Части мицеллы показаны на схеме коллоидной частицы кремнекислоты (рис. 1). Лиофильные К. отличаются от лиофобных строением частиц; они не создают кристаллического ядра, и в разбавленных растворах каждая молекула существует б. или м. самостоятельно или в виде клубка небольшого количества молекул.
Отличительные свойства К. связаны с их ультрамикрогетерогенностью (ультрамикронеоднородностью) и высокой дисперсностью. К. обладают высокой удельной поверхностью (отношение поверхности к объёму) и поверхностной энергией. Это обусловливает значительную поглотительную способность, хим. и каталитическую активность. У ряда веществ, напр. у гипса и отдельных фосфатов, при сильном раздроблении повышается растворимость.
При рассматривании коллоидных растворов невооружённым глазом в проходящем свете и под микроскопом они представляются вполне однородными. В отражённом свете они часто мутны, но характерно, что при боковом освещении пучок световых лучей оставляет светлую полосу, называемую конусом Тиндаля. Свет, рассеиваемый отдельными частицами, виден в ультрамикроскопе, чем пользуются для подсчёта частиц, а также для др. исследований. В ультрамикроскопе (а у суспензии частиц меньше 2 - 3 и в обычном микроскопе) можно наблюдать, что частицы золя находятся в непрерывном движении (броуновское движение), к-рое обусловливает диффузию коллоидов. Однако диффузия коллоидов протекает очень медленно, что связано с размерами их частиц.
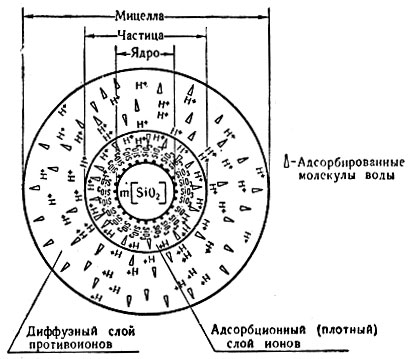
Рис. 1. Схема строения мицеллы кремнекислоты
Вследствие адсорбции электролитов на поверхности коллоидных частиц, они приобретают электрический заряд, но коллоидный раствор в целом электронейтрален, т. к. этот заряд компенсируется ионами диффузного слоя - противоионами (рис. 1). При пропускании постоянного электрического тока через коллоидный раствор частицы движутся к полюсу, имеющему противоположный заряд. Это явление называется электрофорез, в частности, движение отрицательно заряженных частиц к катоду - катафорез. Если частицы неподвижны (осадок, мембрана), то в электрическом поле движется дисперсионная среда, увлекаемая ионами диффузного слоя (электроосмос). Катафорез, электроосмос и аналогичные явления позволяют определить знак заряда частиц и величину их электрокинетического (дзэта) - потенциала. С увеличением концентрации электролитов дзэта-потенциал вначале повышается, а затем, достигнув максимума, при очень низких концентрациях, резко падает. Трёх- и четырёхвалентные ионы и ион водорода способны менять знак заряда частиц (перезарядка). Адсорбция молекул дисперсионной среды на поверхности частиц и связывание молекул растворителя поверхностными ионами покрывает частицы сольватной (в случае воды, гидратной) оболочкой.
Коллоидные растворы, в отличие от суспензий и эмульсий, кинетически устойчивы, т. е. во времени не происходит их расслаивание под влиянием силы тяжести. Слипанию частиц в агрегате препятствует их заряд и сольватация. При снижении дзэта-потенциала до нек-рого предела, называемого критическим, заряд не в состоянии защищать частицы от слипания и происходит их агрегирование. При этом, если возникают достаточно крупные и компактные агрегаты, они выпадают из взвеси и коллоидный раствор разрушается - происходит коагуляция. Минимальная концентрация электролита, обусловливающая коагуляцию, называется порогом коагуляции. Его величина падает с увеличением валентности ионов, а для ионов одной валентности со снижением их гидратации.
Если слипание частиц не сопровождается их осаждением (седиментацией), то происходит повышение вязкости коллоидного раствора, явление аномалии вязкости (изменение вязкости с изменением скорости течения жидкости), а впоследствии застывание (желатинирование). Многие гели обладают способностью под влиянием механического воздействия (встряхивание и т. д.) разжижаться в золи, к-рые через нек-рое время самопроизвольно вторично застывают. Это явление носит название тиксотропии. Во времени (при старении) и под влиянием др. факторов гели могут частично выделять дисперсионную среду. Это явление называется синерезисом. Оно может закончиться полной коагуляцией и седиментацией.
Лиофильные коллоиды не коагулируют. Очень высокими концентрациями электролитов они высаливаются. Нарушение их агрегативной устойчивости в обычных условиях приводит к застыванию или особому явлению, получившему название коацервация (рис. 2) - отделение от золя макроскопических капель, наполненных, в свою очередь, роем ультрамикроскопических и микроскопических капель, содержащих неск. изолированных первичных частиц. Лиофильные коллоиды могут повышать устойчивость лиофобных (стабилизировать их), защищая от агрегирования. Коагулят так же, как продукт высаливания, часто м. б. переведён в устойчивую взвесь отмыванием избытка электролита, добавлением стабилизаторов и т. п. (пептизация). Пептизации часто предшествует набухание - впитывание дисперсионной среды и увеличение объёма осадка. Набухание может происходить без последующей пептизации.
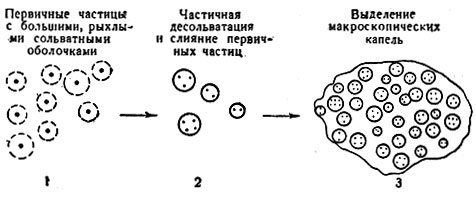
Рис. 2. Схема коацервации
К. широко распространены в природе и имеют большое значение в с.-х. производстве. Белки, крахмал и нек-рые др. основные составные части организма р-ний и ж-ных находятся в коллоидном состоянии. Сложные процессы жизни этих организмов протекают в коллоидных системах. К. играют значительную роль в жизни почв и в обработке почвы (см. Коллоиды почвы, Глины, Ил, Поглотительная способность почвы). Многие с.-х. продукты являются дисперсными системами, и задача их дальнейшей переработки сводится или к стабилизации К. или к их коагуляции. При изготовлении молочных продуктов происходит разрушение водной эмульсии жира, из к-рой состоит молоко. Сок каучуконосов содержит эмульсию каучука. При сахароварении раствор сахара очищается от коллоидных загрязнений.
Литература: Антипов-Каратаев И. и Рабинерсон А., Почвенные коллоиды и методы их изучения, Л., 1930; Думанспий А., Лиофильность дисперсных систем, изд. Воронежского Гос. университета. 1940; его же, Учение о коллоидах, 3 изд., М.- Л., 1948; Жуков И., Коллоидная химия, ч. 1, Л., 1949; Коллоиды в процессах пищевой индустрии. Под ред. А. В. Думанского. Сборник 1, М., 1946; Песков Н. и Александрова-Прейс Е., Курс коллоидной химии, 2 изд., М.-Л.,1948; Путилова И., Руководство к практическим занятиям по коллоидной химии, 2 изд., М.-Л., 1948; Рабинерсон А., Проблемы коллоидной химии, Л., 1937.
Источники:
- Сельскохозяйственная энциклопедия. Т. 2 (Ж - К)/ Ред. коллегия: П. П. Лобанов (глав ред) [и др.]. Издание третье, переработанное - М., Государственное издательство сельскохозяйственной литературы, 1951, с. 624
|
ПОИСК:
|
© AGROLIB.RU, 2010-2022
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://agrolib.ru/ 'Библиотека по агрономии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://agrolib.ru/ 'Библиотека по агрономии'